NOXXON Pharma N.V. berichtet über Finanzergebnisse 2020
“2020 hat NOXXON seine Belastbarkeit demonstriert, indem das Unternehmen seine klinische Entwicklung und Aktivitäten erfolgreich fortgesetzt hat, während es sich der gesundheitlichen Situation angepasst hat. Mit seinem neuen wissenschaftlichen Beirat, der sich aus herausragenden Experten für Bauchspeicheldrüsenkrebs zusammensetzt, und einer starken Cash-Position ist NOXXON nun in einer perfekten Position, um die Entwicklung seines wichtigsten Wirkstoffkandidaten NOX-A12 zu beschleunigen. NOX-A12 zeigte in seiner abgeschlossenen Kombinationsstudie mit Mercks Keytruda® vielversprechende Ergebnisse bei Patienten mit Bauchspeicheldrüsen- und Darmkrebs und ist erst kürzlich in die letzten Phasen einer Phase-1/2-Dosis-Eskalationsstudie in Kombination mit Strahlentherapie bei Patienten mit neu diagnostizierten Gehirntumoren eingetreten. Wir freuen uns auf die Aussichten, die im Jahr 2021 auf NOXXON warten und sind mehr denn je davon überzeugt, dass unser einzigartiger Ansatz, der auf die Mikroumgebung des Tumors abzielt, die Art und Weise der Behandlung von Krebs verbessern kann", sagte Aram Mangasarian, CEO von NOXXON.
Wichtige Ereignisse im Geschäftsjahr 2020 und im bisherigen Verlauf des Jahres 2021
Im Jahr 2020 hat NOXXON erfolgreich 14,5 Mio. EUR eingeworben, was es dem Unternehmen ermöglichte, seine strategischen Ziele voranzutreiben. Die in 2020 und 2021 gesicherte Liquidität in Kombination mit den verfügbaren Wandelschuldverschreibungen hat NOXXONs finanziellen Horizont bis in das zweite Quartal 2022 verlängert. Trotz der COVID-19-Pandemie hat das Unternehmen seine klinischen Entwicklungs- und Investitionsaktivitäten wie geplant mit nur minimalen Verzögerungen fortgesetzt.
Klinische Studie von NOX-A12 + Immuntherapie bei stark vorbehandelten Patienten mit metastasiertem Bauchspeicheldrüsen- und Darmkrebs
Im Jahr 2020 schloss NOXXON die klinische Studie zur Kombination von NOX-A12 mit Keytruda® bei stark vorbehandelten Patienten mit metastasiertem, mikrosatellitenstabilem Bauchspeicheldrüsen- und Darmkrebs ab. Einer der interessantesten Aspekte der endgültigen Top-Line-Daten, die von Prof. Niels Halama auf dem Kongress der European Society for Medical Oncology (ESMO) im September 2020 veröffentlicht wurden, waren die aktualisierten Daten zum Gesamtüberleben. Diese zeigten, dass drei Patienten, wovon zwei bereits ihre vierte Therapielinie bei metastasiertem Bauchspeicheldrüsenkrebs erhielten, mehr als ein Jahr überlebten – einer von ihnen fast zwei Jahre. Insgesamt bestätigten die Daten aus dieser Studie den Wirkmechanismus von NOX-A12 und zeigten, dass NOX-A12 als Monotherapie in das Tumorgewebe eindringt und dort sein Ziel neutralisiert. Dieser Mechanismus ermöglicht es NOX-A12, eine verstärkte Immunantwort innerhalb des Tumors zu stimulieren, wodurch die Mikroumgebung des Tumors immunologisch "heißer" wird. Im zweiten Teil der Studie, als NOX-A12 mit Mercks immuntherapeutischem anti-PD-1-Antikörper Keytruda® kombiniert wurde, erreichten 25 % der Patienten eine Stabilisierung ihrer Krankheit gemäß den iRECIST-Kriterien, obwohl nur 5 % auf ihre vorherige Krebstherapie angesprochen hatten, bevor sie in die klinische Studie von NOXXON aufgenommen wurden.
Klinische Studie von NOX-A12 + Strahlentherapie in neu diagnostizierten Gehirntumorpatienten
NOXXON hat im Jahr 2020 und bis heute seine Phase-1/2-Dosis-Eskalationsstudie von NOX-A12 in Kombination mit Strahlentherapie bei neu diagnostizierten Gehirntumorpatienten erfolgreich vorangetrieben, die in sechs klinischen Zentren in Deutschland durchgeführt wird. Das Unternehmen hat die Rekrutierung von Patienten für die letzte der drei geplanten Kohorten im April 2021 abgeschlossen. Vorläufige Daten aus der ersten Dosisgruppe zeigten Tumorverkleinerungen bei allen drei Patienten, wobei ein Patient ein dauerhaftes – länger als vier Monate andauerndes – objektives Ansprechen (Reduktion des Tumorvolumens >50%) erreichte. Die Top-Line-Daten der zweiten Kohorte werden im Mai 2021 und die der dritten Kohorte später im November 2021 berichtet werden.
Wissenschaftlicher Beirat
Im Februar 2021 hat NOXXON einen wissenschaftlichen Beirat (Scientific Advisory Board, SAB) unter dem Vorsitz von Dr. Jose Saro berufen. Dem SAB gehören vier führende Experten für Bauchspeicheldrüsenkrebs an: Dr. Elena Gabriela Chiorean, Dr. Eileen M. O’Reilly, Prof. Dr. Thomas T. W. Seufferlein und Dr. Daniel D. Von Hoff. Die Bildung und Zusammensetzung des SAB spiegelt die klinische Entwicklungsstrategie von NOXXON wider, da sich das Unternehmen auf den Start einer zweiarmigen Phase-2-Studie bei Bauchspeicheldrüsenkrebs in Europa und den USA vorbereitet.
Herstellung und Wirkstoffbestände
Um den Anforderungen der bevorstehenden klinischen Studien für die Zulassung von NOX-A12 gerecht zu werden, ist NOXXON Investitionsverpflichtungen eingegangen und hat mit der Herstellung von Wirkstoffbeständen von NOX-A12 begonnen. Darüber hinaus hat NOXXON auch mit der Herstellung von NOX-E36 für zukünftige klinische Studien begonnen.
COVID-19
Nach sorgfältiger Beurteilung der Risiken im Zusammenhang mit der weltweiten COVID-19-Pandemie hat das Unternehmen risikomindernde Maßnahmen ergriffen, die die Auswirkungen der Pandemie auf die Organisation minimieren. Insgesamt waren die Auswirkungen der Pandemie auf den Geschäftsbetrieb, die klinischen Studien und die Finanzierung gut zu bewältigen und in ihrem Ausmaß begrenzt.
Starke Cash-Position am 31. Dezember 2020
Am 31. Dezember 2020 verfügte NOXXON über liquide Mittel in Höhe von 10,3 Mio. EUR. Das Unternehmen konnte im Jahr 2020 durch mehrere Privatplatzierungen, durch die Ausübungen von ausstehenden Warrants zum Erwerb von NOXXON-Aktien und durch die Finanzierungsvereinbarung mit Atlas Special Opportunities (ASO) 14,5 Mio. EUR an liquiden Mitteln einwerben. Aus der Vereinbarung mit ASO hat NOXXON noch Zugang zu weiteren Finanzmitteln in Höhe von 12,8 Mio. EUR. Nach dem 31. Dezember 2020 hat das Unternehmen weitere 6,4 Mio. EUR durch eine Privatplatzierung eingeworben. Diese Finanzierungen in Kombination mit den ASO-Mitteln haben den finanziellen Horizont bis in das zweite Quartal 2022 verlängert.
Zusammenfassung der Finanzergebnisse 2020
Sowohl im Geschäftsjahr 2020 (GJ 2020) als auch im Geschäftsjahr 2019 (GJ 2019) hat NOXXON keine Umsätze erzielt. Die Gruppe – NOXXON Pharma N.V. und NOXXON Pharma AG – erwartet keine Umsätze mit ihren in der Entwicklung befindlichen Produktkandidaten, bis die Gruppe entweder eine Lizenzvereinbarung unterzeichnet, die behördliche Zulassung erhält und ihre Produkte vermarktet oder Kooperationsvereinbarungen mit Dritten eingeht.
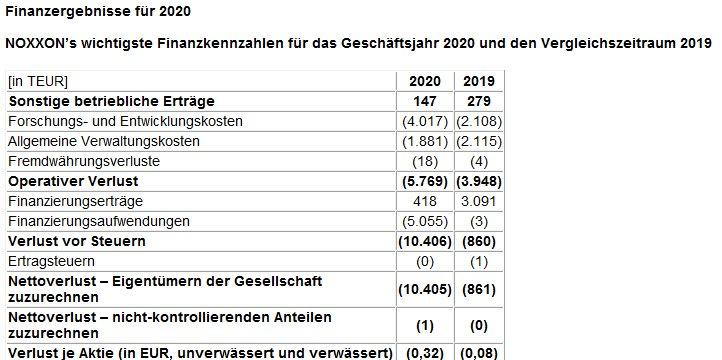
Die sonstigen betrieblichen Erträge sanken von 279 TEUR im GJ 2019 auf 147 TEUR im GJ 2020. Im Jahr 2020 resultierten die sonstigen betrieblichen Erträge aus dem Verkauf von Rohstoffen, erbrachten Dienstleistungen, der Ausbuchung aufgrund des Verzichtes auf Vergütungen und der Ausbuchung von Verbindlichkeiten sowie aus sonstigen Erträgen, die hauptsächlich aus Wechselkursdifferenzen resultierten.
Die Kosten für Forschung und Entwicklung (F&E) stiegen von 2.108 TEUR im GJ 2019 auf 4.017 TEUR im GJ 2020. Der Anstieg der F&E-Aufwendungen im Jahr 2020 im Vergleich zu 2019 war hauptsächlich auf höhere Kosten für die Herstellung von Prüfsubstanz, Dienstleistungen und andere Aufwendungen im Zusammenhang mit klinischen Studien und präklinischen Tests zurückzuführen. Im Personalaufwand sind nicht zahlungswirksame Aufwendungen für aktienbasierte Vergütungen in Höhe von 51 TEUR im Jahr 2020 und 53 TEUR im Jahr 2019 enthalten. Nach Abzug dieser nicht zahlungswirksamen Aufwendungen für aktienbasierte Vergütungen betrug der verbleibende Personalaufwand 622 TEUR im Jahr 2020 und 530 TEUR im Jahr 2019.
Die allgemeinen Verwaltungskosten sanken von 2.115 TEUR im GJ 2019 auf 1.881 TEUR im GJ 2020. Der Rückgang der G&A-Aufwendungen im Jahr 2020 wurde hauptsächlich durch niedrigere Rechts-, Beratungs- und Prüfungskosten und niedrigere Aufwendungen für Öffentlichkeitsarbeit und Investor-Relations im Vergleich zu 2019 verursacht, der teilweise durch höhere Personalkosten kompensiert wurde. Im Personalaufwand sind nicht zahlungswirksame Aufwendungen für aktienbasierte Vergütungen in Höhe von 111 TEUR im Jahr 2020 und 54 TEUR im Jahr 2019 enthalten. Nach Abzug dieser nicht zahlungswirksamen Aufwendungen für anteilsbasierte Vergütungen betrug der verbleibende Personalaufwand 858 TEUR im Jahr 2020 und 741 TEUR im Jahr 2019.
Die Fremdwährungsverluste stiegen von 4 TEUR im GJ 2019 auf 18 TEUR im GJ 2020, was auf ein höheres Einkaufsvolumen in Nicht-Euro-Währungen im GJ 2020 zurückzuführen ist.
Die Finanzierungserträge (alle nicht zahlungswirksam) sanken von 3.091 TEUR im GJ 2019 auf 418 TEUR im GJ 2020. Die Finanzierungserträge resultieren in Höhe von 406 TEUR aus der Ausbuchung von zusammengesetzten derivativen Finanzinstrumenten im Zusammenhang mit der ASO-Finanzierung und in Höhe von 12 TEUR aus der bargeldlosen Ausübung von Warrants.
Bei den Finanzierungskosten in den Geschäftsjahren 2020 und 2019 handelte es sich um nicht zahlungswirksame Finanzierungskosten, mit Ausnahme von Transaktionskosten in Höhe von 123 TEUR im Jahr 2020, die von der Gruppe im Zusammenhang mit der Ausgabe von Wandelschuldverschreibungen getragen wurden. Finanzierungskosten in Höhe von 3.153 TEUR bezogen sich auf die im Jahr 2020 abgeschlossene ASO-Finanzierung und spiegelten Verluste aus der erstmaligen Erfassung von Wandelschuldverschreibungen, aus der Wandlung und aus der Verbuchung zusammengesetzter derivativer Finanzinstrumente sowie Transaktionskosten wider. Des Weiteren entfielen 998 TEUR der Finanzierungsaufwendungen auf die Ausübung von Warrants durch Yorkville, 878 TEUR auf die bargeldlose Ausübung aller verbliebenen ausstehenden Acuitas-Warrants und 23 TEUR auf die Fair-Value-Anpassung der an Kreos, Yorkville und bestimmte andere Investoren ausgegebenen Detachable Warrants sowie 3 TEUR auf Zinsaufwendungen für Leasingverbindlichkeiten.
Im Ergebnis der oben genannten Faktoren erhöhte sich der Verlust vor Steuern der Gruppe von TEUR 860 im GJ 2019 um TEUR 9.546 auf TEUR 10.406 im GJ 2020 (davon operativer Verlust in Höhe von TEUR 5.769 im GJ 2020 im Vergleich zu TEUR 3.948 im GJ 2019, was zu einem Mittelabfluss aus der laufenden Geschäftstätigkeit von TEUR 5.224 im GJ 2020 führte im Vergleich zu TEUR 4.286 im GJ 2019).
Der Ertragsteueraufwand sank von 1 TEUR im Geschäftsjahr 2019 auf null im Geschäftsjahr 2020.
Am 31. Dezember 2020 verfügte die Gruppe über liquide Mittel in Höhe von 10,3 Mio. EUR (im Vergleich zu 1,4 Mio. EUR am 31. Dezember 2019). Der Gruppe gelang es, im Jahr 2020 14,5 Mio. EUR aus verschiedenen Quellen einzuwerben, darunter durch Privatplatzierungen, die Ausübungen von ausstehenden Warrants und aus der ASO-Finanzierungsvereinbarung. Im Jahr 2021 hat die Gruppe bisher weitere 6,4 Mio. EUR aus einer Privatplatzierung aufgebracht. Wichtig ist, dass mit den bei diesen Finanzierungen ausgegebenen Aktien keine Warrants oder andere optionsähnliche Instrumente verbunden waren. Die kontinuierliche Unterstützung von Investoren mit der Bereitschaft, Aktien auf diese Weise zu erwerben, ist für NOXXON von entscheidender Bedeutung, denn dadurch kann die Abhängigkeit von Instrumenten mit dem Potenzial zur Schaffung divergierender Interessen zwischen verschiedenen Gruppen von Investoren verringert werden. Diese Finanzierungen waren essenziell, damit NOXXON die NOX-A12/Keytruda®-Studie bei Patienten mit Bauchspeicheldrüsen- und Darmkrebs abschließen, die NOX-A12/Strahlentherapie-Kombinationsstudie bei Patienten mit Gehirntumoren vorantreiben und die Herstellung von NOX-A12 und NOX-E36 für kommende klinische Studien initiieren konnte. Am 31. Dezember 2019 stand eine beträchtliche Anzahl von Warrants aus, die in Verbindung mit früheren Finanzierungen ausgegeben worden waren. Diese enthalten Verwässerungsschutzklauseln, die den Ausübungspreis und die Anzahl der auszugebenen Aktien betreffen. Im Laufe des Jahres 2020 übte Yorkville einen großen Teil seiner Detachable Warrants aus und Acuitas machte von seinem Recht auf bargeldlose Ausübung für alle seine Warrants Gebrauch. Im Ergebnis wurde die Kapitalstruktur des Unternehmens weniger komplex.
Ausblick 2021
Das aktuelle Budget sieht im Jahr 2021 einen monatlichen Liquiditätsbedarf von ca. 1,5 Mio. EUR vor. Dies beinhaltet alle geplanten Aktivitäten für die laufende NOX-A12-Gehirntumorstudie, die Wirkstoffproduktion und den Studienbeginn der anstehenden NOX-A12-Bauchspeicheldrüsenkrebsstudie sowie der NOX-E36-Studie. Die derzeitigen liquiden Mittel werden voraussichtlich die Finanzierung des Unternehmens bis November 2021 und mit den Mitteln aus der ASO-Finanzierung bis Mai 2022 sichern. Das Unternehmen verfolgt verschiedene Finanzierungsalternativen, um den zukünftigen Budgetbedarf zu sichern, einschließlich der Kontaktaufnahme zu bekannten US-Investoren im Gesundheitswesen, der Beschaffung weiterer Mittel von bestehenden Investoren durch zusätzliche Finanzierungsrunden, der Suche nach strategischen Partnerschaften sowie nach Fusions- oder Akquisitionsmöglichkeiten.
NOX-A12 + Immuntherapie + Chemotherapie bei Patienten mit Bauchspeicheldrüsenkrebs in Zweitlinienbehandlung
Mit ermutigenden Daten aus einer früheren Studie und mit Anleitung des SAB bereitet NOXXON den Start einer zweiarmigen klinischen Studie bei Bauchspeicheldrüsenkrebs vor. Zusätzlich zur Kombinationstherapie von NOX-A12 plus anti-PD-1 wird die Studie zwei verschiedene Standard-Chemotherapien in der Zweitlinienbehandlung testen. Der Beginn der Studie ist für das zweite Halbjahr in 2021 geplant und ihr Abschluss wird für 2023 erwartet. Dieser strategische Ansatz wird NOXXON in die Lage versetzen, das optimale Therapieschema auszuwählen, um in eine randomisierte, kontrollierte Zulassungsstudie überzugehen, die den Antrag auf Marktzulassung im Jahr 2026 und die Zulassung im Jahr 2027 zum Ziel hat.
NOX-A12 + Strahlentherapie bei Patienten mit neu diagnostizierten Gehirntumoren
NOXXONs oberste Priorität ist es, den rechtzeitigen Abschluss der laufenden Phase-1/2-Dosiseskalationsstudie sicherzustellen und im Jahr 2021 Top-Line-Daten zu präsentieren. Mit dem Ziel, zusätzliche Sicherheitsdaten vor dem Start der Zulassungsstudie zu erhalten, bereitet NOXXON derzeit die Erweiterung der Patientenzahlen auf einer der getesteten Dosisstufen vor. In der Erwartung, dass die Daten der laufenden Phase-1/2-Studie die weitere Entwicklung unterstützen, plant NOXXON, im Jahr 2022 eine Zulassungsstudie für NOX-A12 in Kombination mit Strahlentherapie bei Patienten mit neu diagnostiziertem MGMT-Promotor-unmethyliertem Glioblastom im Vergleich zur Standardtherapie zu starten, wobei der erste Zulassungsantrag für 2024 und die Zulassung für 2025 angestrebt wird.
Klinische Pläne für NOX-E36
Mit seiner verbesserten Finanzlage plant NOXXON, die klinischen Studien mit NOX-E36 wieder aufzunehmen. Die Produktion des Wirkstoffs für klinische Studien wurde in Auftrag gegeben und Material für die Studien wird voraussichtlich im zweiten Halbjahr 2021 verfügbar sein. Die präklinischen Arbeiten zum Vergleich von Kombinationsstrategien für NOX-E36 bei soliden Tumoren, um die vielversprechendsten Ansätze zu identifizieren, kommen ebenfalls voran. Das Unternehmen plant, die erste klinische Studie mit NOX-E36-Kombinationen zur Prüfung der Sicherheit im Jahr 2021 zu initiieren.
Der vom Vorstand und Aufsichtsrat am 28. April 2021 verabschiedete Geschäftsbericht 2020 ist auf der Website von NOXXON (www.noxxon.com) verfügbar.
Risikohinweis zu den Zukunftsaussagen
Bestimmte Angaben in dieser Meldung beinhalten zukunftsgerichtete Ausdrücke oder die entsprechenden Ausdrücke mit Verneinung oder hiervon abweichende Versionen oder vergleichbare Terminologien, diese werden als zukunftsgerichtete Aussagen (forward-looking statements) bezeichnet. Zusätzlich beinhalten sämtliche hier gegebenen Informationen, die sich auf geplante oder zukünftige Ergebnisse von Geschäftsbereichen, Finanzkennzahlen, Entwicklungen der finanziellen Situation oder andere Finanzzahlen oder statistische Angaben beziehen, solch in die Zukunft gerichtete Aussagen. Das Unternehmen weist potenzielle Investoren darauf hin, sich nicht auf diese Zukunftsaussagen als Vorhersagen über die tatsächlichen zukünftigen Ereignisse zu verlassen. Das Unternehmen verpflichtet sich nicht, und lehnt jegliche Haftung dafür ab, in die Zukunft gerichtete Aussagen zu aktualisieren, die nur den Stand am Tage der Veröffentlichung wiedergeben.
Die auf Onkologie fokussierte Pipeline von NOXXON wirkt auf die Tumormikroumgebung (TME) und den Krebs-Immunitätszyklus durch Durchbrechen der Tumor-Schutzbarriere und die Blockierung der Tumorreparatur. Durch die Neutralisierung von Chemokinen in der TME wirkt der Ansatz von NOXXON in Kombination mit anderen Behandlungsmethoden schwächend auf die Tumorabwehr gegen das Immunsystem und ermöglicht eine größere therapeutische Wirkung. NOXXONs Lead-Programm NOX-A12 lieferte finale Daten aus einer Kombinationsstudie mit Keytruda® in Patienten mit metastasiertem Darm- oder Bauchspeicheldrüsenkrebs, die im September 2020 auf der ESMO-Konferenz publiziert wurden. Auf der Basis dieser Studienergebnisse, einschließlich der Daten für Gesamtüberleben und des Sicherheitsprofils, sind weitere Studien zur Behandlung von Bauchspeicheldrüsenkrebs in Planung. NOXXON untersucht außerdem NOX-A12 in Kombination mit Strahlentherapie in Hirntumoren. In den USA und in der EU wurde dieser Kombination zur Behandlung bestimmter Hirntumore der Orphan-Drug-Status erteilt. Vorläufigen Daten aus der ersten Kohorte einer Studie von NOX-A12 in Kombination mit Strahlentherapie in neu diagnostizierten Hirntumorpatienten, die nicht von einer Standard-Chemotherapie profitieren würden, zeigten konsistente Tumorrückbildungen. Der zweite TME-Produktkandidat des Unternehmens, NOX-E36, befindet sich in der klinischen Phase 2 und zielt auf das angeborene Immunsystem ab. NOXXON plant, NOX-E36 sowohl als Monotherapie als auch in Kombination bei Patienten mit soliden Tumoren zu untersuchen. Weitere Informationen finden Sie unter: www.noxxon.com
Keytruda® ist eine eingetragene Handelsmarke von Merck Sharp & Dohme Corp.
Noxxon Pharma AG
Max-Dohrn-Strasse 8-10
10589 Berlin
Telefon: +49 30 72 62 47 0
Telefax: +49 (30) 726247-225
https://www.noxxon.com/
Chief Executive Officer
Telefon: +49 (30) 726247101
E-Mail: amangasarian@noxxon.com
Trophic Communications
Telefon: +49 (89) 2388-7730
E-Mail: schweitzer@trophic.eu
![]()